Herstellung von Cultured Meat
Geburt, Fütterung, Schlachtung – seit Beginn der Nutztierhaltung ist dies der Prozess, der den menschlichen Fleischkonsum ermöglicht. Schon jetzt steht ein neuer Fleisch-Produktionsprozess zur Wachablösung bereit: Fleischzucht im Labor. Im Folgenden erfahren Sie, wie die Herstellung Cultured Meat abläuft.
Wie wird Cultured Meat hergestellt?
Die Herstellung von Cultured Meat ist ein komplexer biochemischer Prozess. Im Folgenden haben wir diesen Vorgang vereinfacht und in 7 Schritten zusammengefasst. Klicken Sie auf „Mehr erfahren“, um detailliertere Informationen zu den einzelnen Schritten zu erhalten.
Schritt 1: Gewebeprobe
Ganz ohne tierisches Material kommen die Hersteller von Cultured Meat - zumindest bislang - nicht aus. Zum Züchten von Laborfleisch – egal ob Rind, Huhn oder Schwein - ist ein Gewebestück aus der Skelettmuskulatur erforderlich, das dem Tier unter Betäubung entnommen wird. Die sogenannte Muskelbiopsie, ist ein routinemäßiger tierärztlicher Eingriff – zu Schaden kommt das Tier dabei nicht. Zumal es sich pro Entnahme lediglich um eine 0,5 Gramm schwere Gewebeprobe handelt.
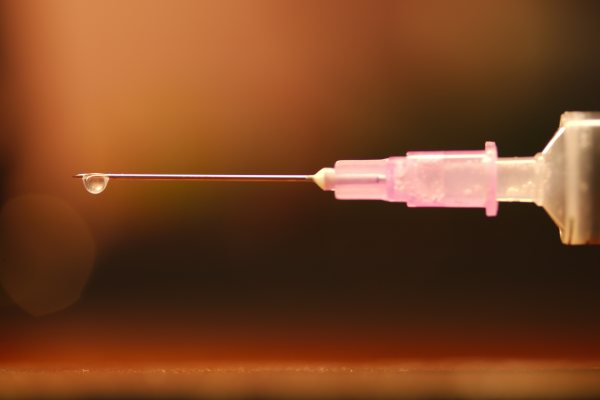
Schritt 2: Isolierung von Stammzellen
Aus besagter Gewebeprobe werden anschließend Myosatellit-Zellen, also Stammzellen, isoliert, aus denen das Laborfleisch später gezüchtet wird. Um sicherzustellen, dass sich diese Stammzellen später in die passenden Zelltypen verwandeln, werden sie einer speziellen Behandlung unterzogen.

Schritt 3: Nährmedium
Um die Proliferation, also die Vermehrung der Stammzellen (-> Spungmarke zu „Wachstum und Vervielfältigung der Stammzellen“), anzuregen, braucht es ein sogenanntes Nähr- beziehungsweise Kulturmedium. Dabei handelt es sich um eine mit speziellen Stoffen angereicherte Lösung, die die Stammzellen unter anderem mit Kohlenhydraten, Eiweiß und Fetten versorgt.
Schritt 4: Bioreaktor
Dieser Prozess findet in einem sogenannten Bioreaktor statt. Dabei handelt es sich um ein Braukessel-ähnliches Gerät, das die für Proliferation und Differenzierung perfekten Umgebungsbedingungen simuliert. Dazu zählt bei der Aufzucht von Säugetier-Stammzellen beispielsweise eine Temperatur von 37 Grad – analog zur Temperatur in vivo.
Schritt 5: Differenzierung
Nun kommt die spezielle Behandlung aus Schritt 2 zum Tragen. Dank dieses Vorgehens differenzieren, also verwandeln sich, die Stammzellen nun in verschiedene Zelltypen, etwa Muskel- oder Fettzellen. Eben in diejenigen Zellen, aus denen sich herkömmliches Fleisch zusammensetzt.
Schritt 6: Fleischaufbau
Solange die Muskel- und Fettzellen im Nährmedium innerhalb des Bioreaktors gedeihen, beschränkt sich ihr Wachstum auf lediglich zwei Dimensionen. Wenn es darum geht, Hackfleisch zu produzieren, reicht das auch aus. Um Steaks zu produzieren, muss das Zellmaterial aber in eine dreidimensionale Form gebracht werden. Dazu haben sich zwei Methoden herauskristallisiert:
Scaffolds (Gerüste): Scaffolds sind Gerüste, aus essbaren beziehungsweise biologisch abbaubaren Stoffen, an denen die Zellen emporwachsen können. Diese müssen die Bildung von Blutgefäßen sowie die Durchblutung fördern, um eine flächendeckende Versorgung der Zellen mit Sauerstoff und Nährstoffen zu gewährleisten, und obendrein dazu in der Lage sein, die Reifung von Gewebe zu unterstützen.
Mehr erfahrenAdditive Fertigung (3D-Druck): Bei der additiven Fertigung wird das Zellmaterial mithilfe eines 3D-Druckers aufeinandergeschichtet, sodass sich am Ende eine dreidimensionale Form ergibt.
Mehr erfahren
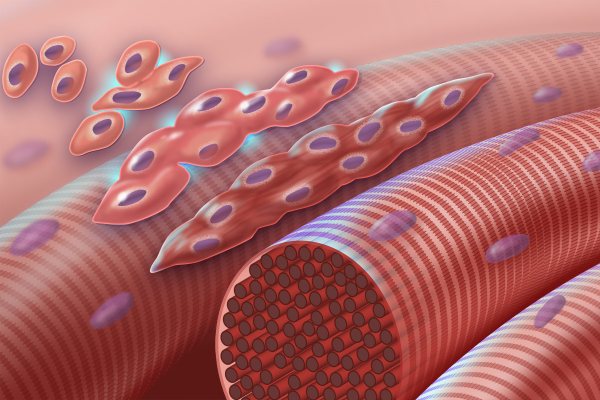
Die Herstellung von Cultured Meat im Detail
Die Herstellung von Cultured Meat umfasst hochkomplexe biochemische Prozesse und erfordert High-Tech-Apparaturen. Wie diese im Detail ablaufen und funktionieren, erklären wir im Folgenden.

Muskelbiopsie
Die sogenannte Muskelbiopsie dient der Gewinnung von Gewebe aus der Skelettmuskulatur des Tieres. Dazu wird das Tier zunächst betäubt, in der Regel mittels Lokalanästhesie. Anschließend wird entweder eine offene Biopsie oder eine Stanzbiopsie durchgeführt.
Bei der offenen Biopsie, die gängigere Methode, wird der entsprechende Muskel mittels Hautschnitt freigelegt. Anschließend wird die Gewebeprobe entnommen und die Wunde zugenäht. Die Alternative ist die sogenannte Stanzbiopsie. Dabei wird eine Biopsienadel zur Entnahme von Gewebe perkutan, also durch die Haut hindurch, in den Muskel eingeführt.
Zelllinien
Um Cultured Meat, Cultured Fish oder andere In-vitro-Nachbildungen herzustellen, braucht es Stammzellinien. Also Stammzellen, die sich in einer Zellkultur unbegrenzt fortpflanzen können. Das besondere an Stammzellen ist ihre Undifferenziertheit. Das heißt, sie können sich je nach Beschaffenheit in verschiedene spezialisierte Zelltypen verwandeln, also differenzieren. Totipotente Stammzellen sind dazu in der Lage, sich in alle im Körper vorkommenden Zelltypen zu differenzieren. Das gleiche gilt für pluripotente Stammzellen, allerdings mit Ausnahme derjenigen in der Plazenta. Multipotente Stammzellen können sich in mehrere spezialisierte Zellen innerhalb einer bestimmten Linie differenzieren. Unipotente Stammzellen können sich dagegen ausschließlich in einen bestimmten Zelltyp verwandeln.
Die perfekte Zellart zur Züchtung von Laborfleisch wären Pluripotente Stammzellen. An dieser Stelle stehen wir aber vor einem ethischen Problem: Das Paradebeispiel für pluripotente Stammzellen sind embryonale Stammzellen, zu deren Einsatz zu Forschungszwecken kontroverse Meinungen herrschen. Eine Alternative musste her: Statt pluripotenten Stammzellen werden inzwischen multipotente Blut- und Hautzellen verwendet. Diese werden in einen pluripotenten Zustand zurückversetzt und sind dadurch in der Lage, sich in deutlich mehr unterschiedliche Zellen zu verwandeln. Diese Zellen werden als induzierte pluripotente Stammzellen (iPSCs) bezeichnet. Alternativ lassen sich aber auch multipotente, nicht-embryonale Stammzellen oder unipotente Vorläuferzellen verwenden – jeweils unter der Voraussetzung, dass sich daraus Muskelzelllinien beziehungsweise Muskelzellen entwickeln.
Stammzellen bringen eine Vielzahl positiver Eigenschaften mit. Dazu zählen:
- Unsterblichkeit,
- Proliferationsfähigkeit, also die Fähigkeit zu Zellteilung und Zellwachstum,
- Unabhängigkeit von Adhärenz, also von der Anhaftung zweier Zellen,
- Serumunabhängigkeit, also von der Verwendung von Blutbestandteilen, sowie die
- einfache Differenzierung in Gewebe
Ob diese Eigenschaften vorhanden sind, variiert allerdings abhängig von der Art der Zelle und ihrer Herkunft. Dementsprechend ist eine Anpassung der In-vitro-Kultivierung an die Erfordernisse der jeweiligen Zelllinie vonnöten. Beispiel Unsterblichkeit: Wegen ihrer sogenannten Telomerkappe - dabei handelt es sich um Nukleotidbasen am Ende der Chromosomen -, die sich bei jeder Teilung verkürzt, lassen sich Zellen nur begrenzt oft teilen. Durch das Induzieren der Pluripotenz lässt sich die Telomerkappe aber so verlängern, dass eine unbegrenzte Zahl von Zellteilungen möglich ist.
Nährmedium
Sobald die Zelllinien etabliert sind, werden sie in ein Kulturmedium getaucht, um sie zur Proliferation (Sprungmarke zur „Proliferation“), also zu Vervielfältigung und zum Wachstum, anzuregen. Kulturmedien versorgen die Zellen mit den erforderlichen Kohlenhydraten, Fetten, Proteinen und Salzen.
Das doppelte Rinderserum-Problem
Und genau hier stießen die Forscher auf ein echtes ethisches und auch finanzielles Problem. Denn das für Stammzellenwachstum wohl wirksamste Kulturmedium war zunächst fötales Kälberserum, das Blut ungeborener Kälber. Um Selbiges zu gewinnen, muss zunächst eine schwangere Kuh geschlachtet werden, ehe das ungeborene Kalb herausgeschnitten und aus seinem noch schlagenden Herzen Blut entnommen wird.
Das ist nicht nur moralisch verwerflich, sondern – zumindest in Deutschland – nur unter besonderen Umständen erlaubt. Dementsprechend teuer – zwischen 400 und 800 Euro - ist fötales Rinderserum. Schätzungen zufolge entfallen auf die Kulturmedien zwischen 55 und 95 Prozent der Herstellungskosten von Cultured Meat. Sowohl aus ethischer als auch aus finanzieller Sicht musste also eine andere Lösung her.
Die Lösung des Nährmedium-Problems
Inzwischen gibt es verschiedene Lösungsansätze für das einstige Rinderserum-Problem. Etwa die Gewinnung der für Teilung und Wachstum der Stammzellen notwendigen Wachstumsfaktoren und Proteine aus Pflanzen. Allerdings sind diese Stoffe meist nur in homöopathischen Dosen enthalten. Die Lösung: synthetische Biotechnologie. Damit lassen sich Stoffwechselwege in die entsprechenden Mikroorganismen implementieren, sodass diese die benötigten Substanzen unbegrenzt herstellen.
Mosa Meat, Hersteller des ersten Labor-Burgers, ist laut eigener Aussage auf eine andere Lösung gestoßen. Und zwar durch genaue Beobachtung der Verwandlung von Stammzellen in verschiedene Muskelzellen. Während dieses Prozesses vermehren sich Proteine, die sogenannten Rezeptoren, auf der Oberfläche der Zelle. Zuvor waren für diesen Prozess offensichtlich Inhaltsstoffe des Kälberserums verantwortlich. Mittels künstlicher Intelligenz und Computermodellierungen fanden die Forscher heraus, welche Inhaltsstoffe des Serums für die Aktivierung der Rezeptoren sorgen und stellten diese selbst her. Damit lässt sich Cultured Meat nicht nur ohne den Gebrauch von fötalem Rinderserum herstellen – auch die Produktionskosten sind dank dieser Entdeckung um das 80-fache gesunken.
Bioreaktoren
Das Zellmaterial wird samt Nährmedium und gegebenenfalls Scaffolds in Bioreaktoren platziert, damit die Zellen wachsen und differenzieren können. Bioreaktoren sind große, brauerei-ähnliche Apparate, in denen die Zellen einer Vielzahl von Umgebungsfaktoren ausgesetzt sind, die zur Förderung der Vermehrung oder Differenzierung erforderlich sind. Die Temperatur des Bioreaktors muss den Bedingungen in vivo entsprechen. Im Falle von Säugetierzellen erfordert dies eine Erwärmung auf 37 Grad Celsius. Die meisten Bioreaktoren werden bei 5 % Kohlendioxid gehalten.
Die Zellen können entweder in kontinuierlichen oder in Fed-Batch-Systemen kultiviert werden. Bei ersterem werden die Zellen in einem kontinuierlichen Prozess beimpft und geerntet, so dass sich immer Zellen im Bioreaktor befinden. Bei Fed-Batch-Systemen werden die Zellen in einem einzigen Zeitraum beimpft, kultiviert und geerntet.
Rührkessel-Bioreaktoren sind die am häufigsten verwendete Konfiguration. Ein Impeller erhöht die Strömung und homogenisiert so das Kulturmedium, während ein Diffusor den Austausch von Sauerstoff in das Medium erleichtert. Dieses System wird im Allgemeinen für Suspensionskulturen verwendet, kann aber auch für Zellen eingesetzt werden, die an einer anderen Oberfläche haften müssen, wenn Mikroträger enthalten sind. Festbett-Bioreaktoren werden in der Regel für adhärente Kulturen verwendet. Sie sind mit Faserstreifen ausgestattet, die zusammen ein Bett bilden, an das sich die Zellen anlagern können.

Das belüftete Kulturmedium wird durch das Bett zirkuliert. In Airlift-Bioreaktoren wird das Kulturmedium mit Hilfe von Luftblasen in eine gasförmige Form gebracht, die dann zwischen den Zellen verteilt wird. Perfusionsbioreaktoren sind gängige Konfigurationen für die kontinuierliche Kultivierung. Sie lassen kontinuierlich mit Milchsäure gesättigtes, nährstoffarmes Medium ab und füllen es mit neuem Medium auf.
Proliferation
Bei der sogenannten Proliferation, auch Zellproliferation genannt, wachsen und vermehren sich die aus der Gewebeprobe isolierten Stammzellen. Ausschlaggebend für die Initiation dieses Vorgangs sind die perfekt abgestimmten Bedingungen im Bioreaktor sowie die im Nährmedium enthaltenen Stoffe. Sobald eine Zelle eine ausreichende Menge an Kohlenhydraten, Proteinen und Fetten sowie anderen im Nährmedium enthaltenen Stoffen aufgenommen hat und entsprechend gewachsen ist, teilt sie sich. Auch die neu entstanden Zellen und deren „Nachkommen“ vermehren sich nach und nach und die Population nimmt exponentiell zu, bis eine ausreichend große Menge an Stammzellen erreicht ist.
Differenzierung
Die Zelldifferenzierung ist der Prozess, bei dem sich die inzwischen vermehrten und gewachsenen, noch unspezifischen Stammzellen in spezifische Zellen verwandeln. Im Fall von Cultured Meat entstehen durch die Differenzierung Muskelzellen, Fettzellen und Gewebezellen.

Bevor es zur Zelldifferenzierung kommt, erfolgt die sogenannte Determination, also die Festlegung des Zelltyps, in den die Stammzelle differenziert. Ausschlaggebend sind hier bestimmte äußere Bedingungen, für die sowohl das Nährmedium als auch der Bioreaktor sorgen müssen. Dementsprechend kommt zur Zelldifferenzierung auch ein anderes Nährmedium zum Einsatz als noch bei der Proliferation.
Im Anschluss an die Determination, bei der sich die Zelle optisch noch nicht verändert, erfolgt die Differenzierung, also die Verwandlung der determinierten Stammzelle in eine spezialisierte Zelle. Dabei ändert sich die Zelle nicht nur äußerlich, sondern – je nach Determination – auch innerlich.
Sobald die Differenzierung startet, beginnen die Muskelfasern zu kontrahieren und Milchsäure zu produzieren. Das ist insofern ein Problem, als dass die Fähigkeit der Zellen, Nährstoffe aufzunehmen und sich zu multiplizieren, unter anderem vom pH-Wert ihrer Umgebung beeinflusst wird. Mit zunehmender Konzentration von Milchsäure in den Medien wird die Umgebung saurer und fällt irgendwann unter den optimalen pH-Wert. Um dies zu vermeiden, müssen die Nährböden in diesem Stadium häufig aufgefrischt werden.
Scaffold
Während seiner Entwicklung aus dem Wachstumsmedium ist das Muskelgewebe zweidimensional. Um es in eine dreidimensionale Struktur zu bringen, werden sogenannte Scaffolds, also Formen, die die Zellen dazu anregen sollen, sich zu einer größeren Struktur zu organisieren, verwendet. Um strukturierte Fleischerzeugnisse herzustellen, müssen die Zellen auf Scaffolds angeordnet werden. In vivo erfolgt dies durch Interaktionen mit der extrazellulären Matrix (ECM), ein dreidimensionales Geflecht aus Glykoproteinen, Kollagen und Enzymen. Die ECM überträgt mechanische und biochemische Signale an die Zelle. Genau diese Merkmale müssen Scaffolds imitieren. Wichtige Eigenschaften der Scaffolds sind:
Porosität
Als Poren werden die verschwindend kleinen Öffnungen auf der Oberfläche des Scaffolds bezeichnet. Sie können auf der Oberfläche des Biomaterials geschaffen werden, um zelluläre Bestandteile freizusetzen, die die Gewebeentwicklung beeinträchtigen könnten. Sie tragen auch dazu bei, dass Gas und Nährstoffe in die innersten Schichten der anhaftenden Zellen diffundieren, was die Entstehung eines "nekrotischen Zentrums" verhindert. Selbiges entsteht, wenn Zellen, die nicht in direktem Kontakt mit dem Nährmedium stehen, aufgrund von Nährstoffmangel absterben.

Gefäßbildung
Das in Pflanzen vorkommende vaskuläre Gewebe enthält die Organe, die für den internen Flüssigkeitstransport verantwortlich sind. Es bildet natürliche Topographien, die eine kostengünstige Möglichkeit zur Förderung der Zellausrichtung bieten, indem sie den natürlichen physiologischen Zustand der Myoblasten nachbilden. Es kann auch beim Gas- und Nährstoffaustausch helfen.

Biochemische Eigenschaften
Die biochemischen Eigenschaften eines Gerüsts sollten denen der ECM ähnlich sein. Es muss die Zelladhäsion durch texturelle Eigenschaften oder chemische Bindungen erleichtern. Außerdem muss es die chemischen Reize erzeugen, die die Zelldifferenzierung fördern. Alternativ sollte das Material in der Lage sein, sich mit anderen Substanzen zu vermischen, die diese funktionellen Eigenschaften aufweisen.
Kristallinität
Der Grad der Kristallinität eines Materials bestimmt Eigenschaften wie die Steifigkeit. Eine hohe Kristallinität kann auf Wasserstoffbrückenbindungen zurückgeführt werden, die wiederum die thermische Stabilität, die Zugfestigkeit (wichtig für die Formerhaltung des Gerüsts), die Wasserbindung (wichtig für die Hydratisierung der Zellen) und den Elastizitätskoeffizienten erhöhen.
Zersetzung
Bestimmte Materialien werden zu Verbindungen abgebaut, die für die Zellen von Nutzen sind, obwohl dieser Abbau auch irrelevant oder schädlich sein kann. Durch den Abbau lässt sich der Scaffold leicht aus dem Endprodukt entfernen, sodass nur noch tierisches Gewebe übrigbleibt, was die Ähnlichkeit mit Fleisch in vivo erhöht. Dieser Abbau kann durch den Kontakt mit bestimmten Enzymen ausgelöst werden, die das Muskelgewebe nicht beeinträchtigen.
Essbarkeit
Wenn die Gerüste nicht aus dem tierischen Gewebe entfernt werden können, müssen sie essbar sein, um die Sicherheit der Verbraucher zu gewährleisten. Es wäre von Vorteil, wenn sie aus nahrhaften Zutaten hergestellt würden.
Geeignete Rohstoffe für Scaffolds
Folgende Rohstoffe werden zur Herstellung von Scaffolds eingesetzt:
Zellulose
Zellulose ist das in der Natur am häufigsten vorkommende Polymer und bildet das Exoskelett der Pflanzenblätter. Da sie reichlich vorhanden ist, kann sie zu relativ geringen Kosten gewonnen werden. Außerdem ist sie vielseitig und biokompatibel.
Chitin
Chitin ist das in der Natur am zweithäufigsten vorkommende Polymer. Es kommt in den Exoskeletten von Krustentieren und Pilzen vor. Da die zelluläre Landwirtschaft versucht, die Abhängigkeit von Tieren zu beenden, ist das aus Pilzen gewonnene Chitin von größerem Interesse.

Kollagen
Kollagen ist eine Familie von Proteinen, die die Grundstruktur des menschlichen Bindegewebes bilden. Es wird normalerweise von Rindern, Schweinen und Mäusen gewonnen. Die zelluläre Landwirtschaft überwindet diese Abhängigkeit durch den Einsatz transgener Organismen, die in der Lage sind, die Aminosäurereste zu produzieren, aus denen das Kollagen besteht.
Mycellium
Mycelium sind die Wurzeln von Pilzen. Anwedner machen sich die Festphasenfermentation zunutze, um Pilzgewebe auf Myzelgerüsten zu züchten.
Nanomaterialien
Nanomaterialien weisen einzigartige Eigenschaften auf der Nanoskala auf. Auch daraus lassen sich Scaffolds fertigen.
Spinning
Immersion Jet Spinning ist eine Methode zur Herstellung von Gerüsten durch das Spinnen von Polymeren zu Fasern.
Additive Fertigung
Eine weitere vorgeschlagene Methode zur Strukturierung von Muskelgewebe ist die additive Fertigung. Diese Technik wurde für industrielle Anwendungen zur Herstellung von Objekten aus Kunststoff, Nylon, Metall, Glas und anderen synthetischen Materialien perfektioniert. Die gängigste Variante des Verfahrens besteht darin, ein Filament schrittweise in Schichten auf ein Bett aufzubringen, bis das Objekt fertig ist. Ein Filament aus Muskelzellen kann zu einer Struktur gedruckt werden, die einem fertigen Fleischprodukt ähneln soll, das dann zur Zellreifung weiterverarbeitet werden kann. Mit Hilfe des 3D-Biodrucks wurde bereits steakähnliches Cultured Meat hergestellt, das aus drei Arten von Rinderzellfasern besteht und eine Struktur aufweist, die der des ursprünglichen Fleisches ähnelt.
